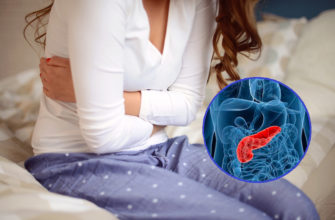
Что такое гипогаммаглобулинемия?
Hypogammaglobulinemia — это заболевание, вызванное низким уровнем иммуноглобулинов или сывороточных антител. Иммуноглобулины являются основными компонентами гуморальной иммунной системы и способны распознавать антигены, вызвать биологический ответ и устранить источник инфекции. HypogammaglobulineMia является наиболее распространенным первичным расстройством сопротивления, к которым выставлены большинство пациентов с уменьшенной резистентностью. Это расстройство может быть диагностировано в детстве или взрослого возраста. Однако начало заболевания обычно происходит во втором или третьем десятилетии жизни, однако клинические симптомы первичной гипогаммаглобулинемии могут появиться любого возраста. Клинические симптомы редки, но они были описаны у пациентов старше 50 лет.
Это заболевание предрасполагает детей и взрослых для рецидивирующих инфекций, аллергии, рака и аутоиммунных заболеваний. Ранее клинические доказательства предполагали, что эти расстройства развиваются в детстве, но теперь они все чаще наблюдаются у взрослых. Общее изменяемое расстройство иммунодефицита (CVID) представляет собой распространенную причину гипогаммаглобулинемии у взрослых, а агамацлобулимемию в сочетании с хромосом X (XCA) является наиболее распространенной причиной в детской популяции.
Симптомы и признаки
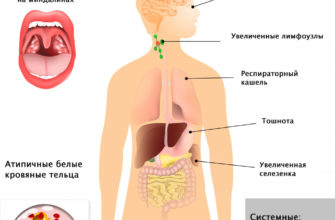
Характерной особенностью гипогаммаглобулинемии обычно является интервью по поводу рецидивирующих, хронических или необычных инфекций. Эти инфекции включают, но не ограничиваются ими собой: бронхит, инфекция ушей (воспаление среднего уха), зубчатые шины, пневмония, бухты (синусит) и кожная инфекция. Такие инфекции могут потенциально повредить органы, ведущие к серьезным осложнениям. Другие симптомы гипогаммаглобулинемии являются хроническая диарея и осложнения после получения живых вакцин. Некоторые симптомы хронических изменений могут быть связаны с рецидивирующей инфекцией. Например, окрасность дыхания, хронический кашель и производство мокроты может указывать на броншиетацию. Боли залива, выделения носа и ринит могут указывать на хронический синусит. Диарея и Storrea могут указывать на расстройства поглощения.
У детей с переходным новорожденным гипогамлульбулинемин (Thn) симптомы обычно появляются 6-12 месяцев после рождения, а симптомы включают частые ушные инфекции, пазухи и легкие. Другие симптомы являются респираторные инфекции, пищевые аллергии, дерматит, инфекции мочевыводящих путей и желудочно-кишечные инфекции.
Причины и факторы риска
Hypogammaglobulinemia может быть первичной или вторичной. Первичные чувствительности иммунитета являются результаты генетических и / или хромосомных неровностей при разработке иммунной системы. Вторичные причины обычно вызваны внешним или приобретенным фактором, например, введение кортикостероидов или иммуносупрессивных лекарств, расстройствами питания, инфекции, химиотерапии, злокачественные опухоли, нефротический синдром, другие метаболические заболевания и опасных сред. Важно различать первичные и вторичные причины гипогаммаклобулинемии для обеспечения надлежащего лечения.
Категория первичных недостатков гуморальной резистентности включает в себя: агамамлобулемию X-связанный, яйцеобразный, синдром Hyper-IgM, селективный / изолированный дефицит иммуноглобулина (Ig) и переходной гипогаммаглаглаглобулинемии рано.
— X-связанная агамагдабуламемия (XCA) или агамамаглавтобулемемия Брутона.
Это первое первичное заболевание иммунодефицита о выявленной генетической причине. Мутация, замеченная в ген Bruton Tyrosine Kinase (TKB), является важным элементом созревания Pre-B. Это приводит к недостаткам клеток плазмы с низким уровнем IG и, следовательно, отсутствие гуморального ответа. Наследование исходной агамамлобулинемии связано с хромосом X, большинство мутаций, и несколько персонажей унаследованы автоматически автоматически.
— Общий вариабельный иммунодефицит (CVID, переменная Pan-Hypogammaglobulinemia).
ОВИН определяется как иммунная дисфункция В-, Т- и дендритных клеток из-за нарушения способности В-клеток дифференцироваться в плазматические клетки, что снижает секрецию иммуноглобулинов. Приблизительно от 25 до 50% пациентов с ОВИН имеют дефект одного гена, который может привести к молекулярной недостаточности, эпигенетическим изменениям, влияющим на экспрессию генов, аномалиям иммунных клеток, таким как повышенный апоптоз В-клеток и нарушение выработки антител. Генетические дефекты включают мутации в ядре, цитоплазме или на клеточной поверхности и могут наследоваться по аутосомно-доминантному или рецессивному типу. Внутренний дефект В-клеток, такой как мутация CD19 в положении 16p11.2, может играть роль, приводя к дефициту CD19. Другой идентифицированный ген представляет собой трансмембранный активатор, модулятор кальция и лиганд взаимодействия циклофилина, который влияет на созревание клеток В. Другая известная мутация представляет собой дефицит взаимодействия лиганда циклофилина с геном TACI в положении 17p11.2. Также были исследованы дефекты гена рецептора фактора некроза опухоли (TNF/TNF), которые также связаны с заболеванием. Другие дефекты Т-клеток с мутациями в ICOS, 2q33 (ICOS-дефицитный OVID), SH2DIA (отвечает за Х-сцепленные лимфопролиферативные синдромы), CD19, CD20, CD21, CD81, BAFF-R (семейство рецепторов фактора некроза опухоли, активирующих В-клетки) и 2 гена, кодирующие ДНК-метилтрансферазу (DNMT3B и ZBTB24). Пациенты с ОВИН и дефицитом IgA имеют общий генетический состав. OVID часто встречается у пациентов с дефицитом IgA 1-й степени родственника, а у некоторых пациентов с дефицитом IgA в более позднем возрасте может развиться пангипогаммаглобулинемия.
— Транзиторная неонатальная гипогаммаглобулинемия (ТНГ).
Это расстройство характеризуется гипогаммаглобулинемией с нормальным ответом антител. Возникает в первые три-шесть месяцев жизни в результате длительного физиологически низкого уровня иммуноглобулинов. У большинства детей уровень Ig нормализуется к трем годам (возрастной диапазон от 2 до 6 лет). Причина неизвестна, но было предложено несколько теорий, в том числе отсутствие стимуляции Т-клетками синтеза В-клеток и антител, подавление продукции IgG материнским IgG, низкий уровень критических цитокинов и наследуемые генетические мутации.
— Дефицит селективного иммуноглобулина А (IgA).
Снижение или отсутствие уровня IgA как в сыворотке, так и в секретируемых формах (IgA 99% IgG. Введение ВВИГ пациентам с дефицитом IgA может вызвать анафилаксию).
Прогноз
Прогноз зависит главным образом от легочных осложнений и злокачественных новообразований. Применение антибиотиков и терапии ВВИГ снизило смертность от бактериальных инфекций. Раннее вмешательство может отсрочить или предотвратить осложнения, но степень замещения IgG для предотвращения осложнений неясна.
Было обнаружено, что пациенты с ТГВ с низким уровнем IgM и IgA выздоравливают медленно, в то время как дети, находящиеся на грудном вскармливании в течение более длительного времени, выздоравливают быстрее. У пациентов с синдромом гипер-IgM смертность является вторичной по отношению к оппортунистическим инфекциям, злокачественным опухолям и заболеваниям печени/желудка.
Осложнения
Легочные осложнения могут привести к сокращению продолжительности жизни даже при раннем обнаружении гипогаммаглобулинемии. Серьезным осложнением является развитие бронхоэктазов, которое встречается примерно у 20% пациентов с рецидивирующими инфекциями в анамнезе. Это может усугубить респираторные симптомы с усилением бронхоспазма, что проявляется обструктивными и/или рестриктивными заболеваниями легких.
Рекомендуется периодическая компьютерная томография высокого разрешения для контроля функции легких. Другим долговременным осложнением является злокачественное новообразование, которое обычно наблюдается на четвертом или пятом десятилетии жизни, и рекомендуется тщательный мониторинг. Введение высоких доз внутривенных иммуноглобулинов на ранних стадиях заболевания может улучшить состояние здоровья и уменьшить легочные осложнения.