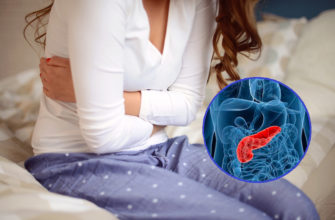
Что такое митохондриальные болезни?
Митохондриальные заболевания — это группа заболеваний, вызванных дисфункцией митохондрий, органелл, вырабатывающих энергию для клеток. Митохондрии находятся в каждой клетке человеческого организма, кроме эритроцитов (эритроцитов), и преобразуют энергию пищевых молекул в аденозинтрифосфат (АТФ), обеспечивающий большинство клеточных функций.
Митохондриальное заболевание приобретает уникальную характеристику как потому, что оно часто передается по наследству, так и потому, что митохондрии очень важны для клеточной функции. Подкласс этих заболеваний, при котором присутствуют нервно-мышечные симптомы, иногда называют митохондриальными миопатиями.
Признаки и симптомы
Симптомы митохондриального заболевания включают:
- плохой рост;
- потеря координации мышц;
- мышечная слабость;
- проблемы со зрением.
- проблемы со слухом;
- трудности в обучении;
- проблемы с сердцем;
- болезнь печени;
- Болезнь почек;
- заболевания пищеварительной системы;
- нарушения дыхания;
- неврологические проблемы;
- вегетативная дисфункция;
- слабоумие.
К заболеваниям, приобретенным с участием митохондриальной дисфункции, относятся:
- диабет;
- Болезнь Хантингтона;
- рак;
- Болезнь Альцгеймера;
- Болезнь Паркинсона;
- биполярное расстройство; шизофрения; тревожные расстройства;
- заболевания сердечно-сосудистой системы;
- саркопения;
- Синдром хронической усталости.
Тело и каждая мутация модулируются различными вариантами генома; мутация, которая может вызвать заболевание печени у одного человека, может вызвать проблемы с мозгом у другого. Тяжесть данного дефекта также может быть высокой или низкой. Некоторые расстройства включают непереносимость физической нагрузки. Дефекты часто в большей степени затрагивают митохондрии и некоторые ткани, приводя к мультисистемным нарушениям.
Как правило, митохондриальное заболевание усугубляется, когда дефектные митохондрии присутствуют в мышцах, мозге или нервах, потому что эти клетки потребляют больше энергии, чем большинство других клеток в организме.
Хотя митохондриальные заболевания сильно различаются по своим проявлениям от человека к человеку, было определено несколько основных клинических категорий этих состояний, основанных на наиболее распространенных фенотипических особенностях, симптомах и признаках, связанных с конкретными мутациями, которые обычно их вызывают.
Причины
Митохондриальные нарушения могут быть вызваны мутациями (приобретенными или унаследованными) в митохондриальной ДНК (мтДНК) или в ядерных генах, которые кодируют митохондриальные компоненты. Они также могут быть результатом приобретенной митохондриальной дисфункции в результате побочных эффектов лекарств, инфекции или других факторов окружающей среды.
Ядерная ДНК имеет две копии на клетку (кроме сперматозоидов и яйцеклеток), одну копию от отца и одну от матери. Однако митохондриальная ДНК наследуется только от матери (за некоторыми исключениями), и каждая митохондриальная органелла обычно содержит от 2 до 10 копий мтДНК. Во время клеточного деления митохондрии случайным образом делятся между двумя новыми клетками. Эти митохондрии производят больше копий, обычно достигая 500 митохондрий на клетку. Поскольку мтДНК копируется во время пролиферации митохондрий, они могут накапливать случайные мутации, явление, известное как гетероплазмия. Если только несколько копий мтДНК, унаследованных от матери, являются дефектными, расщепление митохондрий может привести к тому, что большинство дефектных копий окажется только в одной из новых митохондрий. Митохондриальное заболевание может стать клинически очевидным, когда количество пораженных митохондрий достигает определенного уровня; это явление называется «пороговая экспрессия».
Митохондрии имеют многие из тех же путей репарации ДНК, что и ядра, но не все; следовательно, мутации чаще встречаются в митохондриальной ДНК, чем в ядерной ДНК. Это означает, что нарушения митохондриальной ДНК могут возникать спонтанно и относительно часто. Дефекты ферментов, контролирующих репликацию митохондриальной ДНК (все они кодируются генами ядерной ДНК), также могут вызывать мутации митохондриальной ДНК.
Большая часть митохондриальной функции и биогенеза контролируется ядерной ДНК. Митохондриальная ДНК человека кодирует 13 белков дыхательной цепи, в то время как большая часть из приблизительно 1500 белков и компонентов, нацеленных на митохондрии, кодируется ядром. Дефекты митохондриальных генов, кодируемых ядром, связаны с сотнями фенотипов клинических заболеваний, включая анемию, деменцию, гипертензию, лимфому, ретинопатию, эпилепсию и нарушения развития нервной системы.
В исследовании ученых Йельского университета (опубликовано в Медицинском журнале Новой Англии от 12 февраля 2004 г.) изучалась роль митохондрий в резистентности к инсулину у потомства больных сахарным диабетом 2 типа.Митохондриальное тело в клетках организма ( внутриклеточные липиды). Исследование, проведенное в Центре биомедицинских исследований Пеннингтона в Батон-Руж, штат Луизиана, показало, что это, в свою очередь, частично отключило гены, производящие митохондрии.
Примеры митохондриальных болезней
Примеры митохондриальных заболеваний:
- Митохондриальная миопатия.
-
Сахарный диабет и синдром глухоты:
- Такое сочетание в раннем возрасте может быть связано с митохондриальным заболеванием;
- Сахарный диабет и глухота могут возникать одновременно и по другим причинам.
-
Наследственная оптическая нейропатия Лебера:
- Потеря зрения в раннем возрасте;
- заболевание глаз, характеризующееся прогрессирующей потерей центрального зрения из-за дегенерации зрительных нервов и сетчатки;
- Он затрагивает 1 из 50 000 человек в Финляндии.
-
Синдром Лея, подострая склерозирующая энцефалопатия:
- после того, как ребенок нормально развивается, заболевание обычно начинается в конце первого года жизни, хотя дебют может иметь место и во взрослом возрасте;
- наблюдается быстрое снижение функций, сопровождающееся судорогами, измененными состояниями сознания, слабоумием, нарушением дыхания.
-
Невропатия, атаксия и пигментный ретинит (синдром NARP):
- прогрессирующие симптомы, изложенные с первого взгляда
- слабоумие.
-
Синдром митохондриальной нейрогастроэнцефалопатии (MNGEE):
- кишечная псевдоблокада;
- невропатия.
-
Миоклоническая эпилепсия с синдромом рваных красных волокон (синдром MERRF):
- прогрессирующая миоклоническая эпилепсия;
- «Рваные красные волокна» представляют собой скопления пораженных митохондрий, которые накапливаются в подкожной области мышечного волокна и появляются при окраске мышцы модифицированным трихромом Гомори;
- короткий подъем;
- потеря слуха;
- лактоацидоз;
- непереносимость физических упражнений.
- синдром MELAS (от митохондриальной энцефаломиопатии, лактоацидоза и инсультоподобных эпизодов);
- Синдром истощения митохондриальной ДНК.
Такие состояния, как атаксия Фридрейха, могут поражать митохондрии, но не связаны с митохондриальными белками.
Эпидемиология
Примерно у 1 из 4000 детей к 10 годам развивается митохондриальная болезнь. До 4000 детей в год рождаются с тем или иным типом митохондриального заболевания. Поскольку митохондриальные расстройства включают множество разновидностей и подгрупп, некоторые специфические митохондриальные расстройства встречаются очень редко.
Диагностика
Митохондриальные заболевания обычно обнаруживаются путем анализа образцов мышц, в которых присутствие этих органелл больше. Наиболее распространенными тестами для выявления этих заболеваний являются:
- Саузерн-блоттинг для поиска определенной последовательности ДНК в образце.
- Полимеразная цепная реакция и тестирование на наличие специфических мутаций.
- Последовательность действий.
Лечение
Хотя исследования продолжаются, текущие варианты лечения ограничены; часто назначают витамины, хотя данные об их эффективности ограничены. Пируват был предложен в 2007 году в качестве варианта лечения. N-ацетилцистеин обращает вспять многие модели митохондриальной дисфункции. Было высказано предположение, что для расстройств настроения, особенно биполярного расстройства, N-ацетилцистеин, ацетил-L-карнитин, S-аденозилметионин, коэнзим Q10, альфа-липоевая кислота, моногидрат креатина и мелатонин могут быть потенциальными вариантами лечения.
— Преконцепционная генная терапия.
Перенос веретена, при котором ядерная ДНК переносится в другой здоровый ооцит, оставляя после себя дефектную митохондриальную ДНК, является потенциальной процедурой лечения, которая была успешно проведена на обезьянах. Используя аналогичную технику переноса пронуклеуса, исследователи Университета Ньюкасла под руководством Дугласа Тернбулла успешно пересадили здоровую ДНК из яйцеклеток человека от женщин с митохондриальным заболеванием в яйцеклетки здоровых доноров. В этих случаях возникают этические проблемы в отношении биологического материнства, поскольку ребенок получает гены и молекулы, регулирующие гены, от двух разных женщин. Использование генной инженерии в попытке получить детей, свободных от митохондриальных заболеваний, вызывает споры в некоторых кругах и поднимает важные этические вопросы. В 2016 году ребенок мужского пола родился у матери в Мексике с синдромом Лея с помощью переноса веретена.
В сентябре 2012 года в Соединенном Королевстве были начаты общественные консультации для изучения этических вопросов, связанных с этим вопросом. Генная инженерия человека использовалась в небольших масштабах, чтобы позволить бесплодным женщинам с митохондриальными генетическими дефектами иметь детей. В июне 2013 года правительство Великобритании согласилось разработать законопроект, который легализует «ЭКО с использованием ДНК трех» в качестве лечения для исправления или устранения митохондриальных заболеваний, передающихся от матери к ребенку.
Прогноз
В целом митохондриальные заболевания прогрессируют, и значительное число детей с митохондриальной дисфункцией не достигают совершеннолетия. Скорость прогрессирования может быть переменной и непредсказуемой, но у большинства пациентов в конечном итоге развивается полиорганное поражение.