Создание технологии для долгосрочного поведения жизненно важных репродуктивных клеток посредством криоконсервации значительно расширило возможности репродуктивной медицины. Этот метод был официально признан допустимым для клинического использования в 2012 году, а протоколы IVF с CryoPonstructed (замороженные) теперь широко использовались во всем мире. Crox сохранение ооцитов является основой так называемой Задержка материнства и позволяет создавать криобенцы репродуктивных клеток.
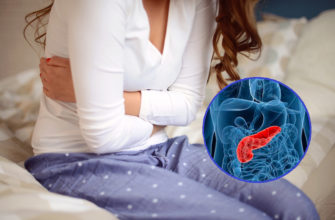
Криоконсервация – это просто заморозка яйцеклеток?

Термин «криоконсервация» означает поведение биологического материала в государственной жизни в очень низких температурах. Но это не обычная замораживание, а очень особенная, сложная и стандартизированная процедура. Он может осуществляться только с использованием специализированного оборудования с очень быстрой функцией восстановления температуры, а затем поддерживать его на строго определенном уровне. Поэтому замораживание и хранение яиц не проводится во всех медицинских учреждениях, только хорошо оборудованные центры рождаемости доказывают эту услугу.
Первоначально, когда оплодотворение in vitro только что было широко введено в клиническую практику, не было четкой необходимости поддерживать репродуктивные клетки. Наконец, даже высокоэффективные схемы гипетоиронической стимуляции не были разработаны, и только 1-2 зрелых ооцитов (яйца) на цикл были получены от одного пациента. Следовательно, существует необходимость в длительном хранении репродуктивных клеток, не теряя жизнеспособность и фертильность.
В начале было попыталось заморозить ооциты в обычный медленный путь. Однако этот способ привел к разрушению значительной части клеток, их клеточные стенки и внутренние структуры были деформированы и были разбиты по результатам ледяных кристаллов. Следовательно, метод медленного замораживания теперь считается недостаточно эффективным, был заменен более продвинутыми методами крио-сохранения. Их приложение позволяет избежать кристаллизации воды, и, таким образом, значительно улучшает выживание ооцитов.
В настоящее время криоконсервация осуществляется в соответствии с 2 основными методами:
- Криптер с предыдущей заменой внутриклеточной воды со специальной криозащитной жидкостью. Гродопроводная клетка медленно вытесняется в специальном растворе, а затем подвергается процедуре замораживания.
- Сайт состоит в ультраструктуре (почти непосредственно), чтобы охладить биоматериал для очень низких температур. В этом случае внутриклеточная вода проходит через стадию кристаллизации и превращается в стеклообразное состояние, а возможность повреждения структур ооцитов и ее генетического материала незначительна.
Сайт считается наиболее эффективной техникой для поддержания максимального количества жизненно важных ооцитов. Основной вклад в его развитие принес японский эмбриолог профессора Масашиге Куяма. Криоконсация его разработана на криотопических подложках и несет имя от его имени или замораживания Китозато. Первый ребенок после оплодотворения стеклянного яйца родился в 1999 году.
Как происходит заморозка ооцита?
Криоконсервация ооцитов состоит в предварительном состоянии от яичников зрелых женщин, функционально полных и подходящих для оплодотворения ооцитов. Это происходит через прокол готовых пузырьков в овуляцию, дата процедуры устанавливает доктора на основе результатов исходного ультразвукового мониторинга. В большинстве случаев загрузка предшествует этап гормональной гипетористой стимуляции для обеспечения созревания большого количества яичных клеток. Однако ооциты, полученные в естественном цикле женщин, также могут быть подвергнуты криооооронзе. Это практикуется, если у пациента противопоказано к использованию даже деликатных протоколов стимула.
Сбор ооцитов для замораживания проходит в стерильных условиях в операционной комнате медицинского центра, обычно под местной анестезией. Пагическая игла тщательно представлена задним вагинальным отверстием, под контролем ультразвука, после очереди к каждому яичкому. Ооциты вместе с фолликулярной жидкостью аккуратно аспирируют в шприц, содержащий питательную среду, после чего процедура считается завершенной.

Сбор ооцитов путем пункции фолликулов
Собранные ооциты сразу же отправляются в эмбриологическую лабораторию, где исследуются и сортируются. Ооциты с видимыми морфологическими аномалиями, видимыми дефектами генетического материала и признаками незрелости выбрасываются и утилизируются. Они не разрешены ни для криоконсервации, ни для использования в текущем протоколе ЭКО, поскольку это сопряжено с высоким риском рождения ребенка с различными генетическими дефектами и аномалиями.
Отобранные клетки помещают в микроконтейнеры в виде пробирок, каждая пробирка имеет четкую маркировку. Затем их замораживают выбранным методом с использованием жидкого азота для создания необходимой низкотемпературной среды. Ооциты хранят в тех же условиях, а температуру поддерживают постоянной на уровне -196 ° C.
Когда применяется технология?
Замораживание ооцитов, их дальнейшее хранение и использование только с письменного информированного согласия женщины. Это решение может быть принято на основании медицинских и социальных соображений. Причем беременность после замораживания ооцитов может наступить только в цикле ЭКО или ЭКО + ИКСИ.
Наиболее частыми причинами криоконсервации репродуктивных клеток являются:
- Сохранение ооцитов, не используемых в текущем протоколе ЭКО. Нередко с помощью стимулированной гиперовуляции получают 10 или более зрелых половых клеток. Из них 4-5 обычно оплодотворяются, при этом имплантируется не более 3 жизнеспособных эмбрионов. Оставшиеся неоплодотворенные ооциты могут быть криоконсервированы по усмотрению женщины, если в медицинском центре есть соответствующие технические возможности. Это позволит в будущих попытках ЭКО избежать гормональной стимуляции и выполнить протокол замороженных ооцитов.
- Создание собственного криобанка репродуктивных клеток для дальнейшей реализации программы отсроченного материнства у здоровых женщин. Такое решение могут принять маленькие пациентки, которые не планируют беременность в ближайшие несколько лет, но хотят избежать риска бесплодия или рождения ребенка с хромосомными аномалиями в будущем. Риск различных мутаций в генетическом материале увеличивается с возрастом, а нежелательная поздняя беременность у женщин в возрасте 37-45 лет связана с повышенной вероятностью рождения ребенка с болезнью Дауна и другими аномалиями.
- Реализация программы сохранения бесплодия. Это шанс получить в будущем генетически материнское потомство у пациентов с диагностированной онкологической патологией. Химиотерапия и лучевая терапия, применяемые у этих женщин, негативно влияют на качество генетического материала ооцитов и могут привести к прекращению созревания фолликулов в яичниках. Если женщина способна самостоятельно вынашивать беременность, имплантируются эмбрионы из оплодотворенных криоконсервированных ооцитов. В противном случае пациентка может воспользоваться услугами суррогатной матери.
- Участие в добровольном донорстве яйцеклеток. В программе могут участвовать только молодые, здоровые женщины, у которых уже есть собственный ребенок.
В последнее время становится все более популярным хранить собственные ооциты. Этот метод используется даже тогда, когда женщина не подвержена риску быстрого истощения запасов ооцитов и не требует цитотоксического лечения.

До какого возраста собирают и замораживают ооциты?
Это один из наиболее часто задаваемых вопросов при посещении врача-репродуктолога. До 35-36 лет риск различных мутаций в наследственном материале репродуктивных клеток считается низким, если только женщина не подвергается воздействию серьезных мутагенных факторов.
Безопасна ли криоконсервация ооцитов?
Не следует ожидать, что абсолютно все криоконсервированные ооциты выживут и останутся полностью функциональными после размораживания. Этого не может гарантировать даже опытный высококвалифицированный репродуктолог на самом современном оборудовании. По статистике выживаемость ооцитов после криопротекции с применением криопротекторов составляет около 85%. Однако в случае витрификации качественных половых клеток этот показатель может достигать 95-98%.
Но ухудшает ли это способность к оплодотворению?
При соблюдении всех технологических аспектов, использовании качественных криоконсервантов и строгом предварительном отборе материала качество размороженных яиц существенно не ухудшится. Кроме того, есть свидетельства того, что застеклованные ооциты производят более жизнеспособные эмбрионы после оплодотворения. Однако эта информация все еще требует окончательного статистического подтверждения.
В среднем степень оплодотворения незамороженных ооцитов составляла 70-79%, и обычно до 41% перенесенных эмбрионов были успешно имплантированы. Это мало чем отличается от цикла ЭКО с нативными (свежими) ооцитами. И в естественных условиях не все яйца безопасно оплодотворяются и приводят к нормально развивающейся беременности. Поэтому считается, что технически грамотная криоконсервация, использование качественных криопротекторов и тщательный отбор ооцитов не меняют их свойств.
Успех протоколов замороженных ооцитов зависит от возраста женщины, состояния ее эндометрия и эндокринного профиля. Качество спермы и комбинация генов, полученных во время оплодотворения, также имеют большое значение. Сам факт криоконсервации не считается важным фактором риска неудачи экстракорпорального оплодотворения.
Перспективность технологии
Ученым еще предстоит установить, как долго женский криобанк остается стабильным. До сих пор в медицинской литературе не описано ни одного случая криоконсервации ооцитов более 10 лет назад. Чаще всего используется замороженный биоматериал 3-5 лет. Однако это не означает, что его нельзя хранить в течение длительного времени. Проще говоря, криоконсервация яиц — это довольно молодая репродуктивная методика, которая уже успешно применяется во всем мире и продолжает совершенствоваться.
Большой интерес представляют протоколы ЭКО плюс ЭКО + ИКСИ с замороженными ооцитами, как собственными, так и донорскими. Они являются основой программ отсроченного материнства и сохранения фертильности у женщин с онкологическими заболеваниями, помогают снизить фармакологическую нагрузку на организм пациентки при повторных циклах ЭКО.